VSEC アプリケーション
アポトーシス細胞由来細胞外小胞の前処理最適化プロトコル
研究背景
英国バーミンガムのアストン大学、アンドリュー・デビット教授の研究室では、アポトーシス細胞由来細胞外小胞(ACdEV)が細胞死の過程でどのように放出され、免疫系へどのようなシグナルを伝達するのかを研究しています。特に、ACdEV が自然免疫細胞をどのように調節するか、その分子メカニズムに関心を持ち、マクロファージの炎症状態に対する ACdEV 表面プロテオームの寄与を中心に解析を進めています。本研究においてEV測定の最適化のためにVSEC-35を使用したワークフローが提案されました。
未結合色素と抗体の除去における新しいワークフローの提案
VSEC-35はEV 解析におけるクリーンアップ工程を大幅に効率化するツールです。
サンプルの濃度と体積を保ったまま未結合色素や抗体を除去できるため、微量サンプルでも安定した測定が可能です。また、1 カラムあたり 50〜100 µL の少量で処理でき、必要な色素・抗体量を抑えられることでコストとサンプルの節約につながります。そして、遠心操作のみで短時間に複数サンプルを同時処理できるため、染色条件の比較や解析を効率よく進められ、EV 研究のスループットを高めます。
VSEC‑35 を使用した バックグラウンドノイズ低減による NanoFCM 測定の最適化
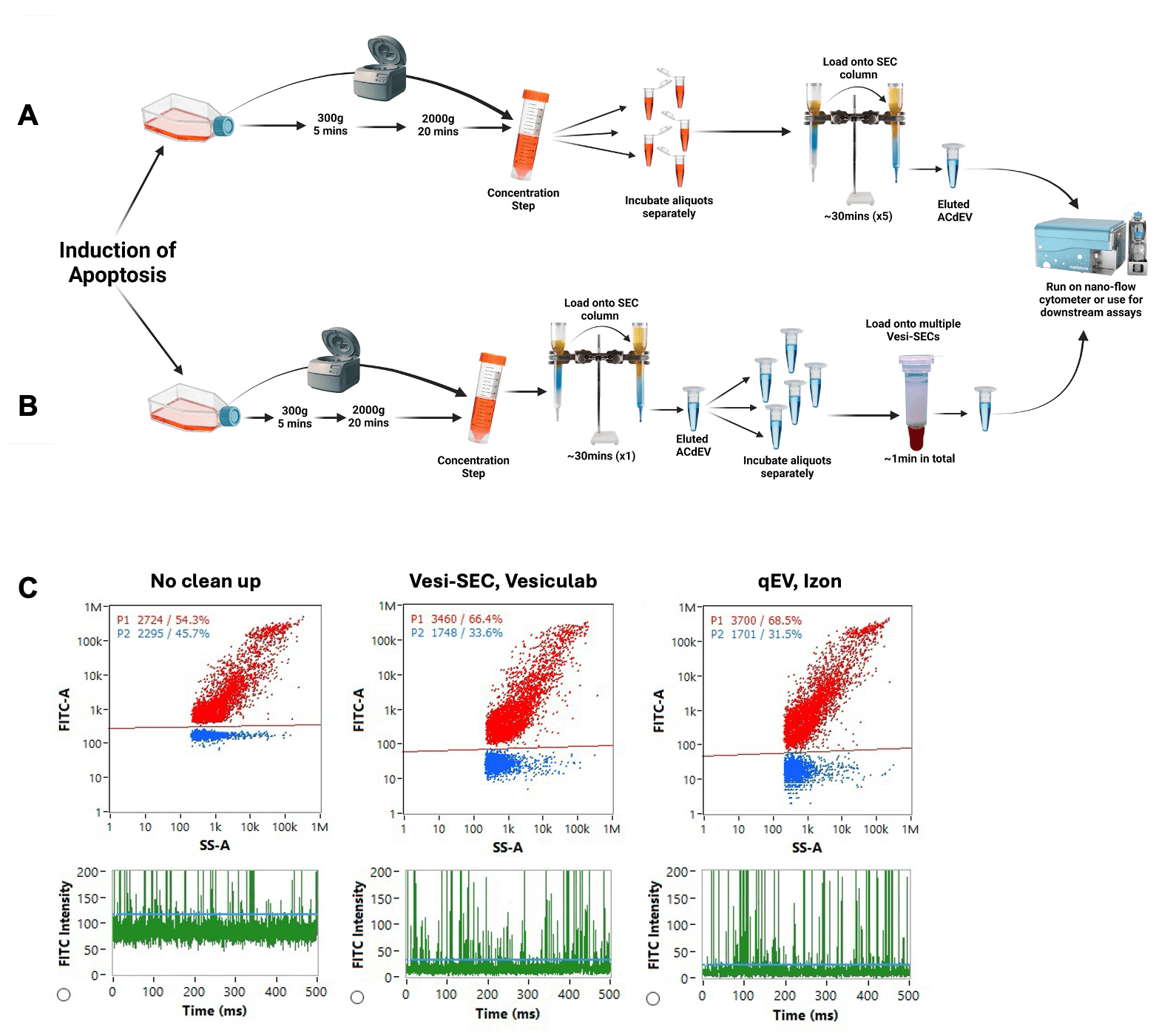
BODIPY™ FL マレイミド標識 ACdEV のバックグラウンドノイズの低減において、qEV original と同等の効率を示しています。
A) 従来のワークフローの課題
qEVの分離システム SEC(EVのサイズ排除クロマトグラフィー)を繰り返して同時に ACdEV を分離し、染料/抗体をクリーンアップすると時間がかかり、大量のサンプルが必要になります。
B) VSEC‑35 を組み込んだ効率的ワークフロー
qEVの分離システム SEC (EVのサイズ排除クロマトグラフィー)による ACdEV 分離に続いて、 VSEC-35(遠心分離SECカラム) による未結合色素/抗体のクリーンアップにより、ワークフローの効率が向上します。
C) NanoFCM による評価:背景ノイズが約 4 倍低減
過剰な BODIPY™ FL マレイミド色素によって引き起こされる FITC チャネルのバックグラウンド ノイズが約 4 倍減少したことからもわかるように、VSEC-35(遠心分離SECカラム) は過剰な未結合蛍光体を除去する点で qEV original と同等の効率性があることがわかります。
サンプル濃度を薄めずバックグラウンドノイズだけを除去
VSEC-35はサンプルの濃度と容量を維持しながらサンプルのクリーンアップを行うことができます (表1)。さらに、VSEC-35カラム 1 個あたりに必要なサンプル容量は最小限 (50 ~ 100 μL) であるため、必要な色素/抗体の量を減らすことができます。
VSEC-35(遠心分離SECカラム)を染料/抗体インキュベーションワークフローに組み込むことで、ACdEV の短時間・高スループット処理が可能になり、各 ACdEV サンプルから得られる情報が最大化されます。
| サンプルの準備 | ACdEVの濃度 (BODIPY™+粒子/mL) | クリーンアップ手順前の ボリューム | クリーンアップ手順後に 収集されたボリューム |
|---|---|---|---|
| クリーンアップなし | 1.94E+10 | 該当なし | 該当なし |
| VSEC-35 (遠心分離SECカラム) | 2.46E+10 | 100μL | 100μL |
| qEV original | 6.58E+9 | 500μL | 100μL |
表 1: VSEC-35(遠心分離SECカラム) と qEV original によるサンプル量と濃度
VSEC-35(遠心分離SECカラム)と qEV originalによるサンプルのクリーンアップにより、以前は隠れていた集団が明らかになり、BODIPY™+ 粒子/mL の濃度がより高くなったと報告されています。濃度はフローナノアナライザー (NanoFCM) で測定しました。 (N = 1)
蛍光標識色素のバックグラウンドノイズ除去
研究背景
フィリップス大学マールブルクの EV コア施設では、血漿・尿・腹水など多様なバイオフルイドから分離した EV を対象に、蛍光標識抗体や脂溶性染料を用いた表現型解析を行っています。
これらの解析では、未結合の抗体や染料を確実に除去することが、測定の明瞭性と再現性を高めるうえで極めて重要となります。
そこで、多様なバイオフルイドを扱う際に EV の完全性と純度を確保するため、VSEC‑35 カラムを利用したプロトコルを用いてEV分析の感度と特異性を大幅に向上させ、高スループットかつ信頼性の高い表現型特性解析を実現しました。
蛍光色素由来のノイズを除去し、 EVのシグナル検出を強化
VSEC‑35 は、蛍光標識 CD63 抗体や親油性色素で染色した EV から、未結合の抗体・色素を効率的に除去し、ナノフローサイトメトリー解析の明瞭性と信頼性を大幅に高めるクリーンアップツールです。
抗体標識 EV のシグナル検出の向上
腹水由来 EV を APC 標識 CD63 抗体で染色し、その後 VSEC‑35 で処理することによって余分な抗体を除去し、未処理時と比べて蛍光強度(APC)と側方散乱(SSC)のシグナルが明確に増加し、検出感度が向上します。
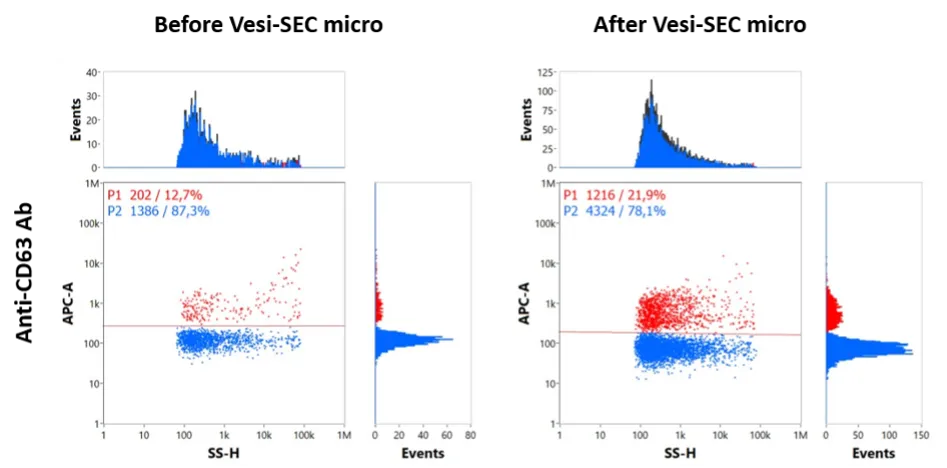
EV は差動遠心分離とタンジェンシャルフローろ過(TFF)を組み合わせて腹水から分離し、その後 SECカラムを用いたサイズ排除クロマトグラフィーで精製しました。約 5×10⁸ 個の粒子を APC 標識 CD63 抗体(クローン H5C6, BioLegend)とともに 4°C で一晩インキュベートし、均一な反応を得るために継続的に撹拌しました。
VSEC カラム処理の前後でナノフローサイトメトリー解析を行い、二変量ドットプロット(APC × SSC)を比較したところ、処理後には蛍光シグナルが明瞭に増強され、未結合抗体の除去による検出感度の向上が確認されました。
脂質膜標識 EV のシグナル検出の向上
腹水由来 EV を親油性色素で染色し、その後 VSEC‑35 で処理することによって未結合色素の除去を行うことができ、フローサイトメトリーによる検出感度の向上が確認されました。
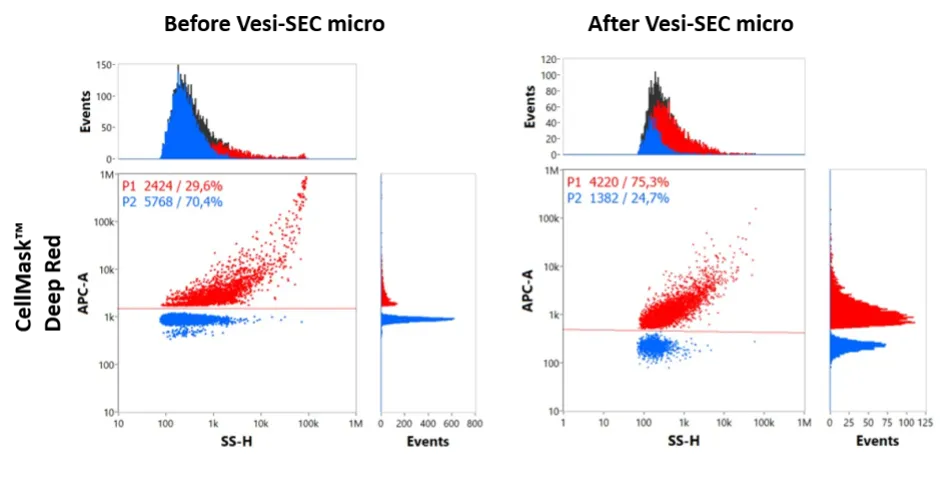
約 5×10⁸ 個の粒子を蛍光標識親油性色素(CellMask Deep Red, Thermo Fisher Scientific))とともに 4°C で一晩インキュベートし、室温で 1 時間インキュベートしました。
VSEC カラム処理の前後でナノフローサイトメトリー解析を行い、二変量ドットプロット(APC × SSC)を比較したところ、処理後には蛍光シグナルが明瞭に増強され、未結合色素の除去による検出感度の向上が確認されました。
VSECカラムを使用することで、過剰な抗体や脂溶性染料を効率的に除去でき、ナノフロー解析の明瞭性と信頼性が大幅に向上します。これによりEV 分析の感度と特異性が高まり、最小限の手間でより正確なフェノタイピングが可能になります。
細胞培養上清由来EVのSP-IRIS分析
VSEC-35 Midiで分離されたEVサンプルは、SP-IRIS(Interferometric Reflectance Imaging Sensor)により高精度に定量評価されました。以下は代表的なエクソソームマーカーに基づく粒子濃度の測定結果です。
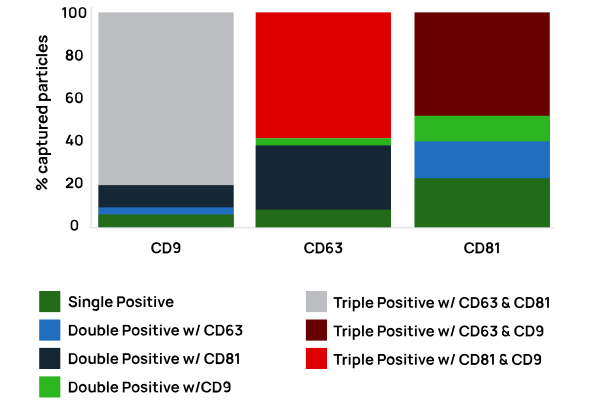
| マーカー | 濃度(particles/mL) |
| CD9 | 3.23 × 10¹⁰ |
| CD63 | 4.60 × 10¹⁰ |
| CD81 | 6.10 × 10¹⁰ |
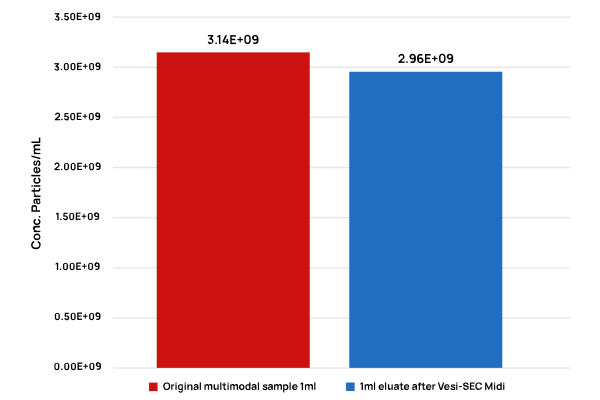
VSEC-35 Midi 処理後のナノ粒子サンプルの濃度と回収率
これらの濃度値は、粒子の物理的サイズと光学的特性に基づく定量により得られたもので、EV分離の高効率性と粒子の構造保持性を示しています。
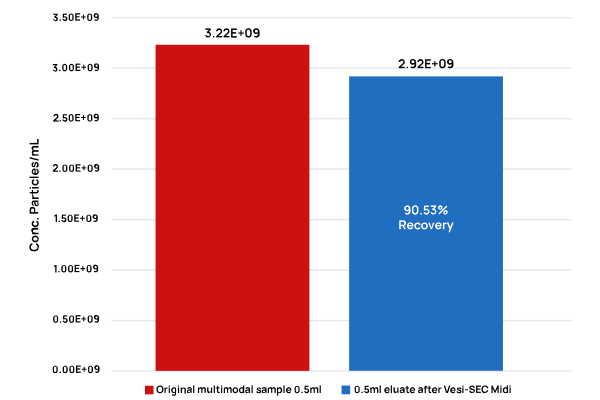
▲高回収率 >90% を達成し、粒子の形態・機能も保持(VideodropによるILM解析)
VSEC-35 Midi このような用途におすすめです
🧪 下流解析への前処理(プロテオミクス、RNA解析、免疫検出、機能解析など)
🔬 細胞培養上清からのEV単離(未処理または濃縮済みサンプルに対応)
🦠 ウイルスの精製(複雑なサンプルからの迅速分離)

