ECM 細胞外マトリックス ~ECMの構成と幹細胞の制御~
細胞を支持し、組織の形成と機能を制御するバイオマテリアル
![]() ーもくじー
ーもくじー
細胞外マトリックス(ECM)は、生物の細胞外に存在する不溶性物質であり、すべての組織や臓器に存在する非常に複雑で動的な3次元構造です。
ECMを構成する成分や付着する細胞の量、割合は人体のさまざまな組織によって異なり、多様な様相を示します。組織工学的な観点においても、ECMは組織の形態形成や分化、恒常性維持に必要な生化学的、生体力学的な手がかりを提供すると同時に、細胞接着の支持体として機能し、臓器や組織の構造的・機能的完全性における重要な役割を担っています。
また、ECMはその特性から再生医療や組織工学における多様な応用が模索されています。臓器の再建や再生に使用する材料を作製するために脱細胞化組織を使用すると、特定の生物学的および機械的なシグナルを与えるため、細胞によって本来の組織で見られる複雑な微小環境を模倣することができます
ここではこれらECMの基本的な概念やその構成要素、幹細胞ニッチにおける役割や精製医療における応用的役割など、生体組織に不可欠なECMに関する情報について解説をします。
ECMの構成要素
多様な構成要素とその働き
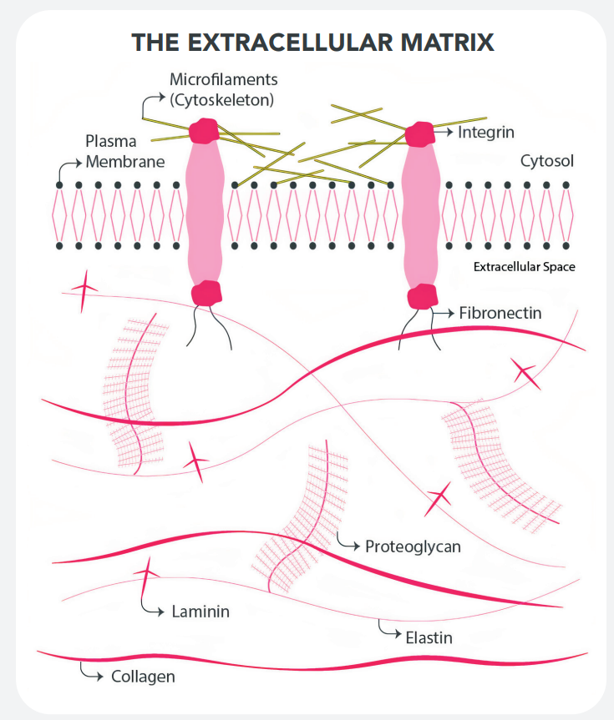
細胞外マトリックスは不溶性繊維と可溶性分子の組み合わせで構成されています。
コラーゲンとエラスチンは繊維状のタンパク質で、常在細胞に構造的な支持を与え、組織に弾力性を与えます。ラミニンやフィブロネクチンなどの多接着性糖タンパク質は、ECMへの細胞接着を仲介します。グリコサミノグリカンとプロテオグリカンは、ECMの他の構成要素が浸されたハイドロゲルの形成に関与する高分子です。
ECMを構成するタンパク質や多糖類、およびそれに付着する細胞の量、割合、組織は、人体のさまざまな組織によって異なります。例えば、骨や歯では、リン酸カルシウムなどのミネラルが沈着することでECMが石灰化します。
- コラーゲン (Collagen)
コラーゲンは、細胞外マトリックスに存在する豊富な繊維状タンパク質であり、ECMの主要な構造要素です。その種類は多様であり、28種類のコラーゲンが報告されており、それぞれが異なる構造、性質、機能を持っています。I型コラーゲンは最も一般的であり、皮膚や骨、腱や靭帯に多く含まれ、体内の90%を占めています。II型コラーゲンは軟骨に多く存在し、可逆的に圧縮される特性があります。III型コラーゲンは血管や消化管、子宮の平滑筋など変形性の組織に存在します。
コラーゲンは3本のポリペプチド鎖からなる3重らせん構造を持ち、この構造にはグリシンが重要な役割を果たしています。コラーゲンの変異は構造形成の遅れや修飾の増加を引き起こし、遺伝性結合組織疾患の特徴となります。 - エラスチン (Elastin)
エラスチンは、動脈、肺、心臓、皮膚など、体の様々な組織に存在し、弾力性線維の主要成分として働くことで組織が負荷に耐えることを可能にします。
トロポエラスチンは可溶性のエラスチン前駆体であり、細胞外に分泌され、細胞膜近くの弾力線維に集まります。このトロポエラスチン分子は相互に架橋し、大きな繊維状のネットワークとエラスチンの層を形成します。エラスチンの合成障害や不溶性繊維のタンパク質分解が起こると、重要な臓器の正常な発育と機能に影響を与え結果として重大な臨床病態を引き起こす可能性があります。 - グリコサミノグリカン(GAG: Glycosaminoglycan)
グリコサミノグリカン(GAG)は、負の電荷を持つ非分岐の多糖鎖であり、硫酸基またはカルボキシル基の存在によって特徴付けらます。GAGにはコンドロイチン硫酸、デルマタン硫酸、ヘパラン硫酸、ヘパリン、ケラタン硫酸、ヒアルロン酸(またはヒアルロナン)の6種類の高分子が含まれています。
ヒアルロン酸は最も単純なGAGであり、硫酸基を持ちません。他のGAGは細胞内で合成されてエキソサイトーシスによって放出されるのに対し、ヒアルロン酸は細胞膜で合成され、直接細胞表面から放出されます。GAGは非常に硬く、親水性の鎖を持ちます。そのため、タンパク質のような他の長い構造体が折りたたまれて球状の立体配座になるのと異なり、伸びたままになる傾向があります。そのためこれらの高分子は大きな体積を占め、低濃度においてもハイドロゲルを形成します。 - プロテオグリカン (Proteoglycan)
プロテオグリカンは、タンパク質のコアにGAGが共有結合した鎖で構成され、3次元構造を形成していますが、その構造形態はさまざまです。結合組織に含まれるデコリンは1本のGAG鎖しか持ちませんが、関節軟骨に多く含まれるアグリカンは100本以上のGAG鎖を持っています。また、ヒアルロン酸はタンパク質との結合を持たないGAGですが、アグリカンと相互作用することで大きな凝集体を形成し、関節軟骨組織が圧縮荷重に耐えられるようにしています。
いくつかの研究では、成長因子の機能に対するプロテオグリカンの重要性が強調されており、このタンパク質はほとんどの細胞において、増殖、細胞分化、およびその他の機能を制御し、プロテオグリカンがマトリックスの他の構成要素を刺激するほか、細胞外マトリックスの受容体として機能する事例もあるとされています。 - フィブロネクチン (Fibronectin)
フィブロネクチンは、脊椎動物に広く存在する大型の接着性糖タンパク質であり、細胞の細胞外マトリックスへの接着や細胞移動を調節します。フィブロネクチンは二量体の形で存在し、サブユニットがジスルフィド結合によって結合します。さらに、フィブロネクチンはコラーゲン、フィブリン、ヘパリンなどの細胞外物質や特定の膜受容体と相互作用することができます。 - ラミニン (Laminin)
ラミニンは、α、β、γの3本のポリペプチド鎖からなる多接着性糖タンパク質であり、これらの組み合わせにより多様な形態を形成します。ラミニンはコラーゲンやヘパラン硫酸を含む他の分子と相互作用し、細胞受容体とも結びついて細胞と細胞外マトリックスをつなぐ橋として機能します。
そのほかにも細胞の分化や移動、接着、増殖、アポトーシスにラミニンが重要な役割を果たし、細胞分化の段階や特殊な機能の実行に関与することが知られています。
幹細胞ニッチとしてのECM
幹細胞の表現型の確立と維持、分化を行うための微小環境
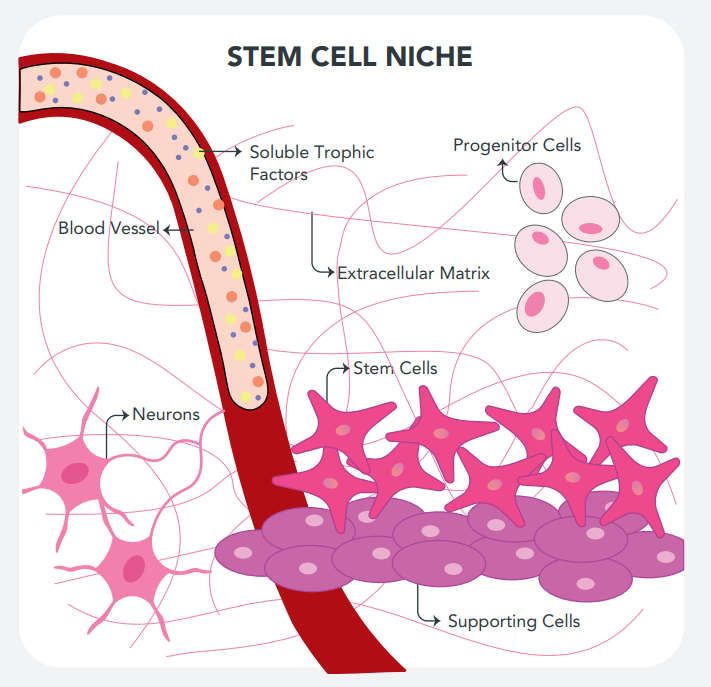
組織の発生と恒常性維持におけるECMの本質的な側面は幹細胞のニッチとして機能する能力です。この微小環境では幹細胞の表現型の確立と維持、分化が行われます。
幹細胞ニッチは、常在細胞、可溶性因子、高分子など、細胞の行動制御に干渉する様々な成分、および構造的な成分で構成されています。常在細胞は組織によって様々な種類があり、接着分子、代謝産物、パラクリンシグナルや神経細胞シグナルを介して幹細胞に作用することができます。内分泌シグナルは、血管を通してニッチに到達します。構造成分は、幹細胞と支持細胞の間の空間的なコンフォメーションや、細胞外マトリックスの接着分子を通じて、幹細胞を制御します
ECMはその分解とリモデリングを通じて、ニッチにおける細胞の活性化と放出に作用します。ECMのバイオメカニクスや組成などのいくつかの特性は、放出後の組織におけるこれらの幹細胞の移動と分化を制御します。変化したニッチや老化したニッチは、幹細胞の特性を維持することが困難です。
ECMが保存された脱細胞化組織を用いて行われたいくつかの実験では、幹細胞の特性を制御する上でECMが重要な役割を果たすことが直接的に示されました。これらの研究において脱細胞化した組織から得られた天然のECM足場が、ECMが由来する組織に存在するタイプの細胞への幹細胞の分化をうまく誘導しました。このような特性から組織工学における脱細胞化臓器の使用が著しく増加しています。
幹細胞
幹細胞は複製や自己再生、特殊な細胞への分化を行うことができ、体内の臓器や組織機能おいて発生、成長、維持、修復に不可欠な役割を果たしています。これらの細胞は未分化であり、生体の修復システムとして機能し他の細胞を補充することができるため、幹細胞培養を用いた組織工学的アプローチは再生医療の分野において大きな注目を集めています。
幹細胞はその分化能力や「可塑性」を反映する「効力」、あるいは発生段階を意味する「由来」によって識別され命名されます。由来が異なると細胞の力や自己再生能力、作用機序が異なる場合があります。したがって、由来に基づき、胚性幹細胞(ESC)、成体幹細胞、人工多能性幹細胞(iPSC)の3つのカテゴリーに大別されます。さらに、分化能の違いから、「全能性幹細胞」「多能性幹細胞」「単能性幹細胞」などのグループに分類することができます。
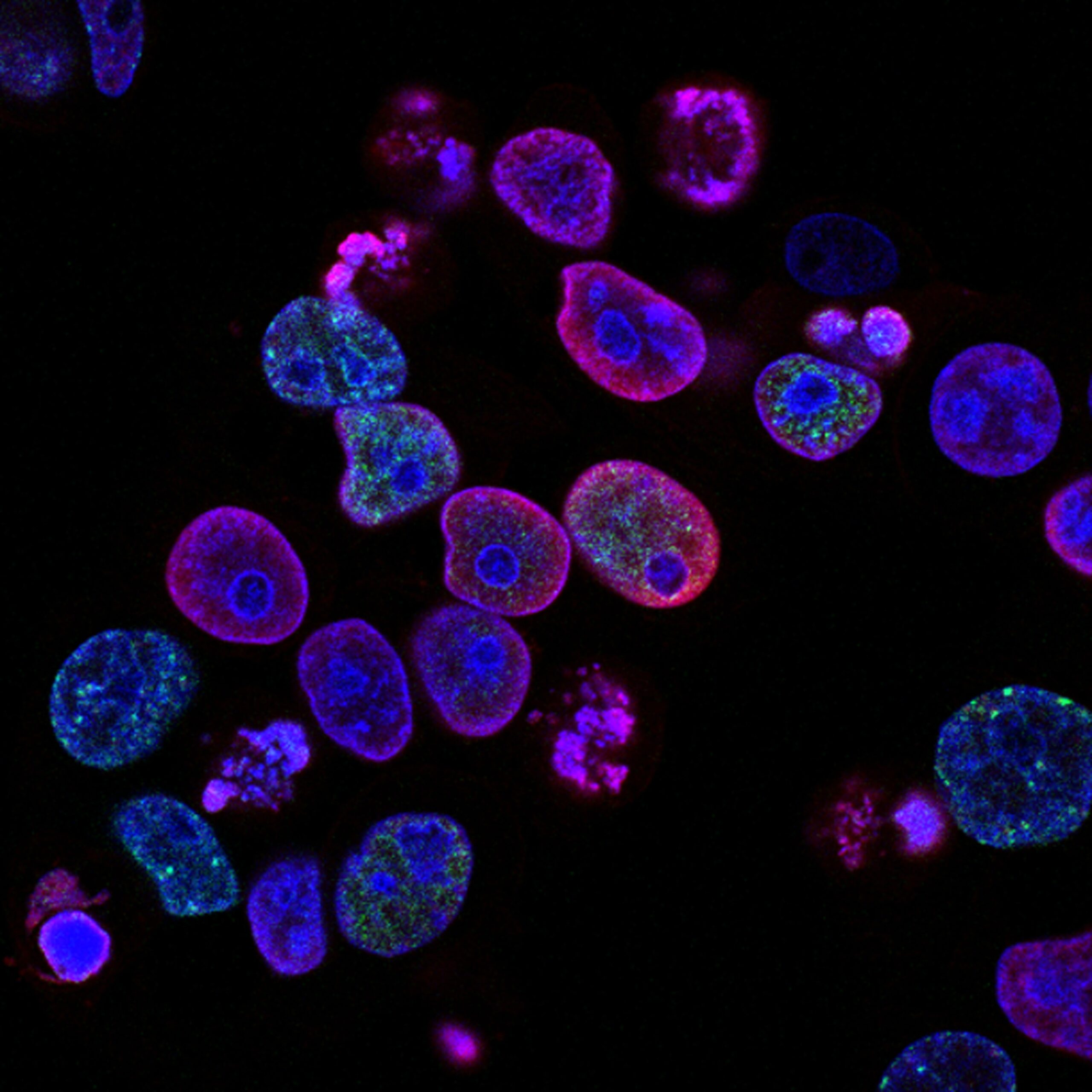
再生医療におけるECMの利用
組織工学における機能的組織形成への展望
ECMは組織の形成に重要な因子であり、臨床および前臨床の研究で広く利用されており、組織培養プラスチックのコーティングから組織や臓器の再建のための誘導モデルまで様々な応用があります。ECMはin vivoでの新しい機能的組織の形成を促進し、組織工学や再生医療において複雑な組織や器官の再構築に役立つ建設的リモデリングを可能にします。ECMは創傷治癒や再生能力などのメカニズムに関与していますが、ECM足場がリモデリングを促進する具体的なメカニズムは、組織の発生と恒常性で起こる一連のプロセスを含め、まだ完全に解明されていません。
脱細胞化ECMの活用
脱細胞化ECM(dECM: Decellularized ECM)は機械的な支持体ならび細胞の移動、付着、分化を促進する材料として機能し、血管、心臓弁、角膜、気管、膀胱、腎臓、肝臓、肺、心臓などの組織を商業および研究目的で再現することに成功しています。脱細胞化技術には、化学的、物理的、酵素的な手法がありますが、いずれの方法においても、脱細胞化の質を高めるためには、本来の構造を保持し、細胞成分を最大限除去することが不可欠です。
ECMの利用に関心が高まっている背景には、細胞の微小環境を再現できる合成足場の作製に関連する課題があります。ECMベースの生物学的足場は、脱細胞化プロセスによって生成されます。この技術は、ECMの構造、生化学的特性、生体力学的特性を維持しながら、ECMから元の細胞やDNAなどの遺伝物質を除去し、患者の細胞を再増殖させ、カスタマイズされた組織や臓器を作ることを目標としています。
細胞培養用のECM搭載ハイドロゲル
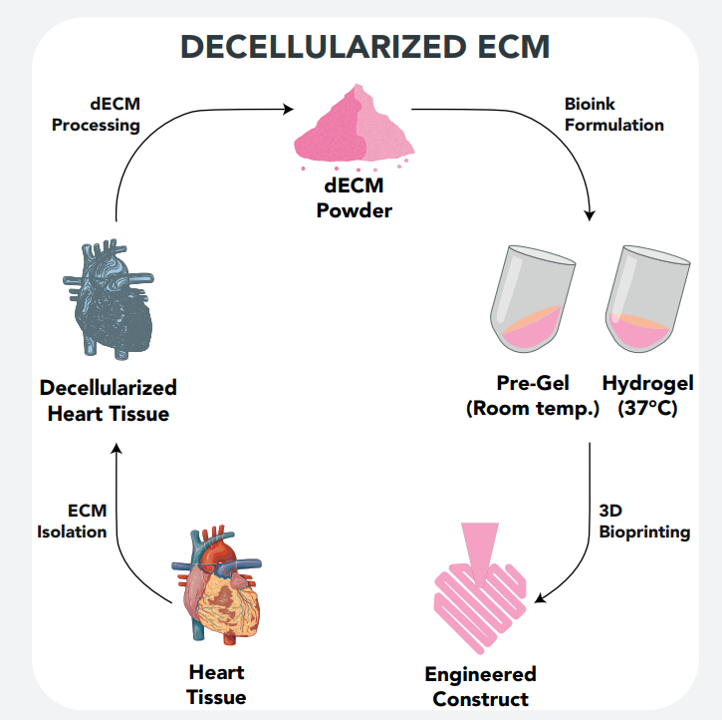
近年、dECMと機能性ハイドロゲル(バイオインク)との連携が進み、3D組織のバイオプリントおける有望なツールとして研究が行われています。ECMをバイオインクに組み込むことで、さまざまな組織タイプの細胞の増殖や分化に高度にバイオミメティックな環境を提供することができます。
dECMベースのバイオインクにおいて、脱細胞化の方法や脱細胞化に使用する組織および臓器の選択、組織を得る動物などが最終的な特性に影響を与えます。脱細胞化工程の後に加工されたdECMはパッチやゲルとして使用するほか、使用前に粉末状に還元して使用することができます。さらに、dECMベースの材料に合成ポリマーを組み合わせることで、バイオマテリアルの特性を調整することができます。特に機械的な耐久性を向上させることが可能であることは興味深いアプローチです。
dECMバイオインクの主な供給源の一つはブタ由来の組織であり入手が容易で大量に入手することができます。また、ヒト由来としては脂肪吸引手術によって得られる脂肪組織が一般的です。Jangら(2016年)はブタ心臓のdECMバイオインクを使用して、心機能を改善するための3Dパッチを作製しました。このバイオインクは心臓前駆細胞とハイドロゲルを組み合わせたものであり、天然の心臓組織の生体力学的特性に対応する天然微小環境を模倣するように設計されました。プリントされたバイオ構造体は、高い細胞生存率と心臓前駆細胞の活発な増殖をサポートし、心筋分化を促進しました。
ECMには生理活性分子が存在するため、これれらのバイオマテリアルは幹細胞の増殖と分化を可能にし、再生足場や組織作製の有望な戦略としての選択肢となる可能性があります。
まとめ
ECMは細胞を支持し、組織の形成と機能を制御するために重要な役割を果たす細胞外の複合体です。細胞とECMの相互作用は生体組織の発育、維持、修復において不可欠であり、健康な組織構築や病態の理解にも重要です。
TissueLabsのMatriXpecハイドロゲルは15種類の組織に対応した幅広いラインナップをそろえており、研究におけるさまざまな要望に対応します。さらに材料を一層ずつ積み重ねることで複雑で精密な構造物を製作するバイオ3Dプリンター技術を組み合わせることにより、細胞に必要な条件を備えた構造物をプリントし、組織再生技術の向上に活用することが可能です。
参考文献
Badylak, S. F. The extracellular matrix as a biologic scaffold material. Biomaterials vol. 28 3587–3593 (2007). Bonnans, C., Chou, J. & Werb, Z. Remodelling the extracellular matrix in development and disease. Nat. Rev. Mol. Cell Biol. 15, 786–801 (2014). Brown, B. N. & Badylak, S. F. Extracellular matrix as an inductive scaffold for functional tissue reconstruction. Transl. Res. 163, 268–285 (2014). Dzobo, K., Motaung, K. S. C. M. & Adesida, A. Recent Trends in Decellularized Extracellular Matrix Bioinks for 3D Printing: An Updated Review. Int. J. Mol. Sci. 20 (2019). Ferraz, F. B. & Fernandez, J. H. Integrinas na adesão, migração e sinalização celular: associação com patologias e estudos clínicos. RCFMC 9, 25–34 (2014). Gattazzo, F., Urciuolo, A. & Bonaldo, P. Extracellular matrix: A dynamic microenvironment for stem cell niche. Biochimica et Biophysica Acta (BBA) - General Subjects vol. 1840 2506–2519 (2014). Godfrey, M. Extracellular matrix. Asthma and COPD 211–218 (2002) doi:10.1016/b978-012079028-9/50097-1. Hynes, R. O. & Naba, A. Overview of the matrisome--an inventory of extracellular matrix constituents and functions. Cold Spring Harb. Perspect. Biol. 4, a004903 (2012). Jang, J. et al. Tailoring mechanical properties of decellularized extracellular matrix bioink by vitamin B2-induced photo-crosslinking. Acta Biomater. 33, 88–95 (2016). Kusindarta, D. L. & Wihadmadyatami, H. The Role of Extracellular Matrix in Tissue Regeneration. in Tissue Regeneration (ed. hay El-Sayed Kaoud, H. A.) (IntechOpen, 2018). Lammi, M., Piltti, J., Prittinen, J. & Qu, C. Challenges in Fabrication of Tissue-Engineered Cartilage with Correct Cellular Colonization and Extracellular Matrix Assembly. International Journal of Molecular Sciences vol. 19 2700 (2018). Pati, F. & Cho, D.-W. Bioprinting of 3D Tissue Models Using Decellularized ExtracellularMatrix Bioink. Methods Mol. Biol. 1612, 381–390 (2017). Pereira, A. L. A. et al. O papel das proteínas da matriz extracelular e das metaloproteinases em carcinomas de cabeça e pescoço: uma atualização bibliográfica. Rev. Bras. Otorrinolaringol. 71, 81–86 (2005). Roughley, P. J. & Lee, E. R. Cartilage proteoglycans: structure and potential functions. Microsc. Res. Tech. 28(5), 385-97 (1994). Yue, B. Biology of the Extracellular Matrix. Journal of Glaucoma vol. 23 S20–S23 (2014).
関連製品:バイオ3Dプリンター

TissueStart(ティッシュスタート)
ミクストルーサー式バイオ3Dプリンター
最高のコストパフォーマンスと多様なニーズに対応した
次世代バイオ3Dプリンター

TissueRay(ティッシュレイ) バイオ3Dプリンター
ステレオリソグラフィシステムによる
次世代ハイレゾリューションバイオ3Dプリンター
様々な組織培養に対応可能!消耗品も数多く取り扱いがございますので、ご研究に合わせて、ぴったりの製品をお選びいただけます。

アプリケーションノートをダウンロードいただけます
TissueLabsアプリケーションノートvol.2
「ECM 細胞外マトリックス ~ECMの構成と幹細胞の制御」
アプリケーションノート「ECM 細胞外マトリックス ~ECMの構成と幹細胞の制御」を公開しております。
ぜひダウンロードいただきご研究にお役に立ていただけますと幸いです。
▼ ご質問はご気軽に 下記ボタンよりお待ちしております ▼

