医学の進歩におけるゼータ電位測定の重要な役割

細胞外小胞(EV)、リポソーム、脂質ナノ粒子(LNP)などのナノ粒子は、医学の進展に大きな可能性を秘めています。これらのナノ粒子が医療応用において有効で安全であることを保証するためには、詳細な特性評価が不可欠です。その際、見過ごされたり、不正確に測定されがちな特性評価の一つが、ゼータ電位です。
コロイド系の安定性におけるゼータ電位の理解
ゼータ電位は、ナノ粒子の安定性に関する貴重な情報を提供します。これは、粒子の表面電荷と周囲の媒質との相互作用を反映しているからです。具体的には、ゼータ電位は、コロイド系における粒子の滑り面での電位の測定です(下図1参照)
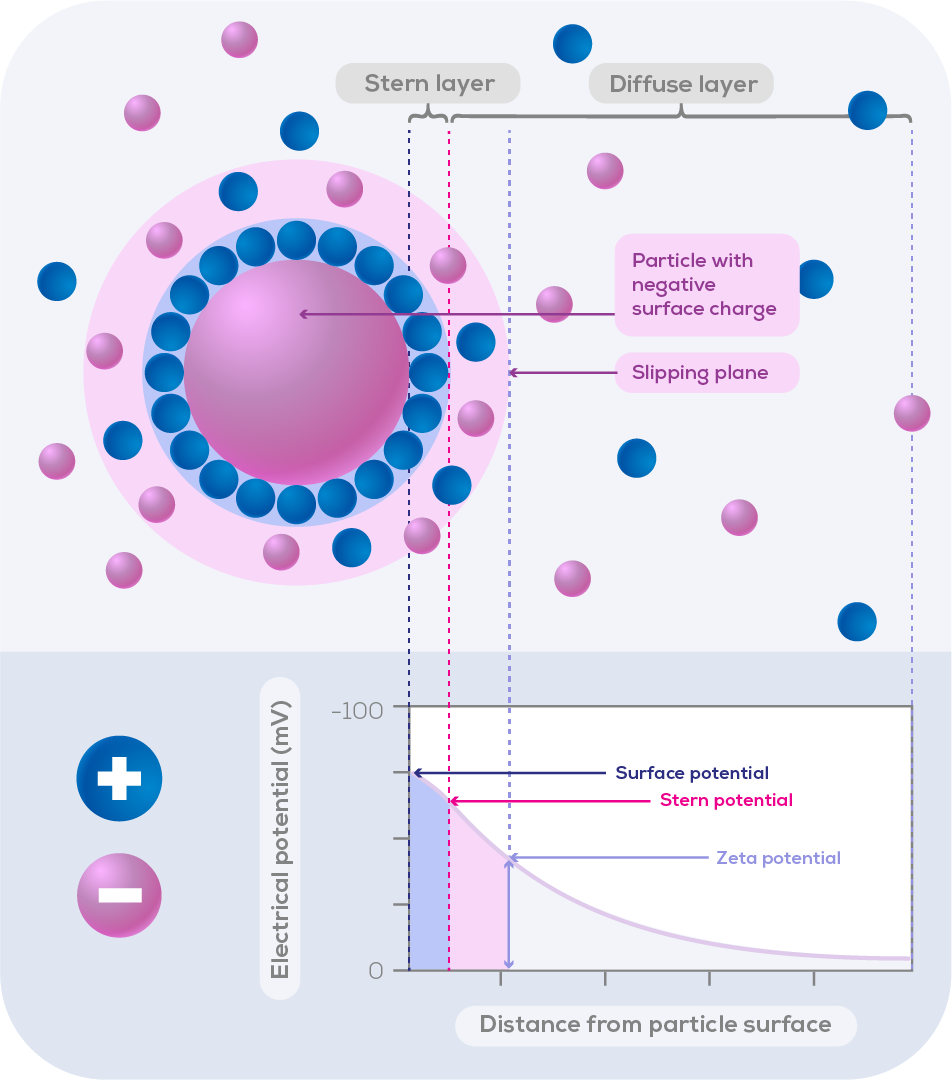
コロイド系とは、ある物質が連続的な「分散」媒質の中に分散している状態を指します2。コロイド粒子間の引力が粒子の凝集や凝固を引き起こす可能性があるため、安定性は非常に重要です。この粒子の凝集を防ぐためには、高解像度のゼータ電位測定が必要となります。
安定したコロイド系では粒子が均等に分布しますが、静電的影響や立体効果で凝集や相分離が発生することがあります。治療目的では均一な分散が重要で、ゼータ電位の測定が安定性の予測に役立ちます。Exoidでは、単一粒子測定技術(TRPS)を用いて、独自の単一粒子ベースで粒子毎のサイズとゼータ電位の測定を同時に取得できます。
ナノ粒子の安定性におけるゼータ電位の役割と治療への影響
ナノ粒子のゼータ電位を測定することで、表面電荷や安定性に関する情報が得られます。安定したナノ粒子は、時間経過に伴ってサイズ、形状、分散を維持しますが、不安定な粒子は凝集して沈殿します。ゼータ電位の大きな値は粒子間の静電反発力が強く、安定した分散を示します。逆に小さい値は反発力が弱く、凝集しやすくなります。治療法の開発では、ゼータ電位の測定が最適化と規制遵守に不可欠です。測定によってナノ粒子の安定性を確認し、治療効果を最大化する条件を整えることができます。
細胞外小胞(EV)の治療効果の最適化
細胞外小胞 (EV) は非侵襲的診断と標的治療に有望であり3、ゼータ電位測定はその安定性と治療の可能性を理解するために重要です。EVのゼータ電位を測定することで、調製方法を最適化し、安定性や細胞相互作用を向上させ4、臨床応用の効果を高められます。最適化されたゼータ電位を持つEVは凝集しにくく、ターゲット細胞への送達効率が向上します。強いゼータ電位は安定した保存をサポートし5.6、品質管理指標としても役立ちます。
ワクチンの安定性と保存期間の確保
ワクチンの安定性と保存期間には、ゼータ電位の測定が重要です。ゼータ電位の絶対値が大きいほど、粒子の反発力が強まり、凝集のリスクが低下し、ワクチンの有効性が長期間維持されます。ゼータ電位を活用してワクチンの配合を最適化し、様々な条件下で安定性を保つことができます。
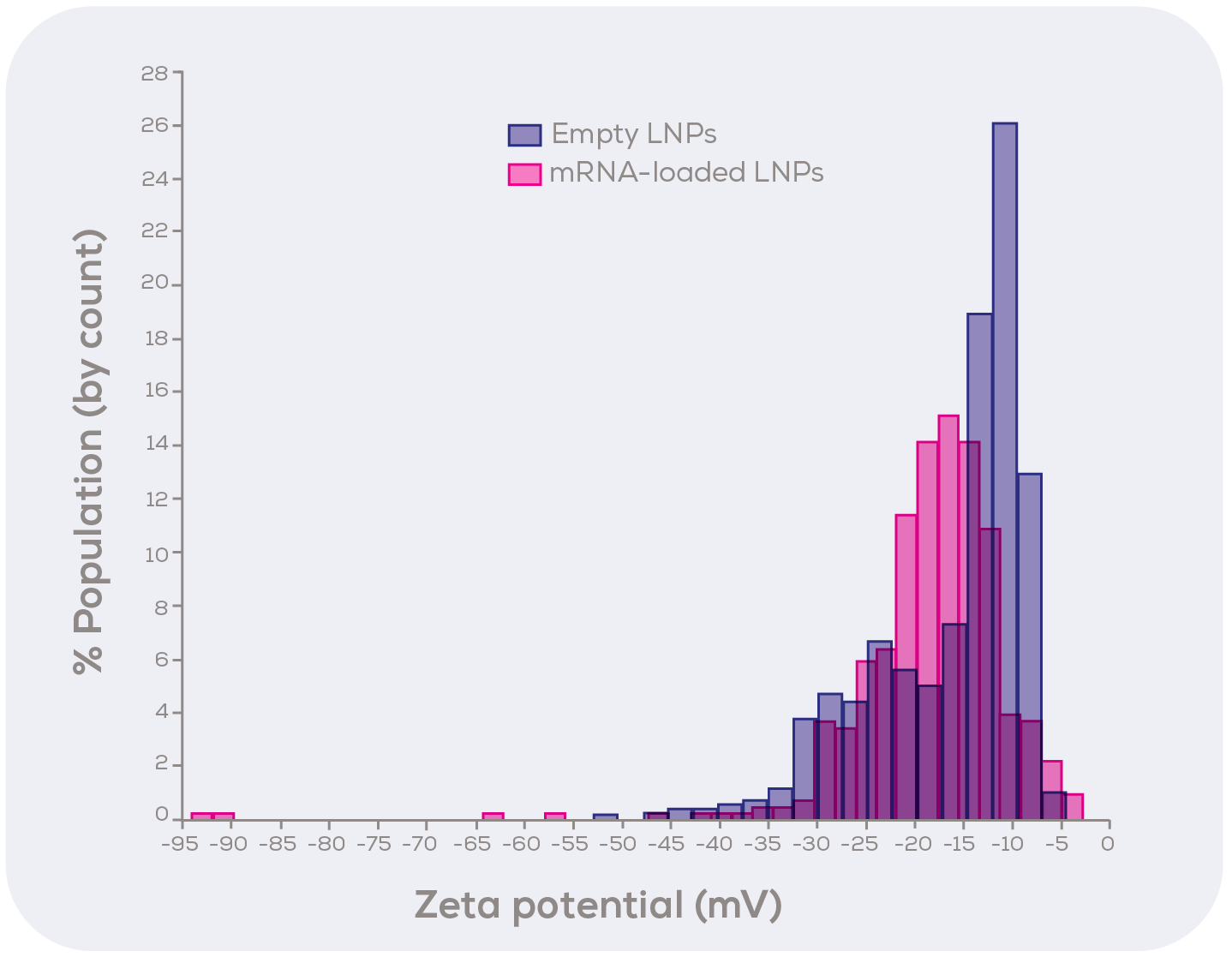
脂質ナノ粒子(LNP)においても、ゼータ電位測定によって安定性が確認され、SARS-CoV-2のmRNAワクチンに使用されました。Exoidを使用した測定では、Empty LNPのゼータ電位が –10 ± 1.1 mV、mRNAを充填したLNPが –17 ± 1.1 mVと示され、負に帯電したmRNAが原因と考えられます。この結果は、Exoidによる高解像度なゼータ電位測定能力を示し、サンプル間の比較に有意な情報を提供します。
ゼータ電位と遺伝子治療における考慮事項
ゼータ電位は、ワクチンやEVの研究開発、遺伝子送達ベクターの設計において重要です。高いゼータ電位を持つナノ粒子は、遺伝子物質の安定性を確保し、ターゲット細胞への効率的な送達を可能にします。正の電荷を持つナノ粒子は、負の電荷を持つ細胞膜との結合を促進しますが、過剰な正の電荷は細胞毒性を引き起こす可能性があるため、バランスが重要です。ゼータ電位の評価は、非特異的相互作用を抑え副作用を減らし、遺伝子治療の精度を高めます。
ゼータ電位:ナノ医療分野における貴重なツール
ゼータ電位の測定は、生物学的ナノ粒子の安定性、効力、安全性を確保するために不可欠です。ゼータ電位を理解し、最適化することで、研究者はナノ粒子の性能を向上させ、規制要件を満たし、革新的な医療治療の開発を進めることができます。Exoidは、ゼータ電位測定の信頼性と正確性を提供するプラットフォームであり、ナノ医療分野の研究者にとって非常に貴重なツールとなっています。
References
- Williams PM. Zeta Potential. Encyclopedia of Membranes. Published online 2016:2063-2064. doi:10.1007/978-3-662-44324-8_612
- Hunter RJ. Zeta Potential in Colloid Science: Principles and Applications. Academic Press, 1981.
- Rupert DLM, Claudio V, Lässer C, Bally M. Methods for the physical characterization and quantification of extracellular vesicles in biological samples. Biochimica et Biophysica Acta (BBA) – General Subjects. 2017;1861(1):3164-3179. doi:10.1016/j.bbagen.2016.07.028
- Midekessa G, Godakumara K, Ord J, et al. Zeta potential of extracellular vesicles: toward understanding the attributes that determine colloidal stability. ACS Omega. 2020;5(27):16701-16710. doi:10.1021/acosmega.0C01582
- Jeyaram A, Jay SM. Preservation and storage stability of extracellular vesicles for therapeutic applications. AAPS Journal. 2018;20(1):1-7. doi:10.1208/S12248-017-0160-Y
- Gelibter S, Marostica G, Mandelli A, et al. The impact of storage on extracellular vesicles: a systematic study. J Extracell Vesicles. 2022;11(2).doi:10.1002/JEV2.12162
- Antoniou V, Mourelatou EA, Galatou E, Avgoustakis K, Hatziantoniou S. Gene therapy with chitosannano particles: modern formulation strategies for enhancing cancer cell transfection. Pharmaceutics. 2024;16(7):868. doi:10.3390/pharmaceutics16070868