qEV20が新登場

細胞外小胞(EV)は、in vivo, in viro を問わず複雑なサンプル中に存在するため、これまで抽出が困難とされていましたが、qEVは効率性、信頼性、純度から、EV研究における重要なステップである「抽出」分野のベンチマークとなっています。
近年はエクソメアやスーパーメア(EVより小さなサイズの非小胞粒子)、遺伝子治療用のアデノ随伴ウイルス(AAV)のへの関心が高まっており、一方でこれらのアプリケーションは、既存のqEVカラムの抽出範囲を下回る粒子サイズであるため、これらに対応できる新たなカラムが切望されていました。
そして、新たにqEV20を発売し、これまで未開拓だった領域への挑戦を行います。
qEV20による効率的な微粒子抽出
qEV20では、既存のqEV35よりも効率的に微粒子を抽出できます。
図1 では抽出効率を確認するために、サイズが既知であるカルボキシル化ポリスチレン粒子(CPC)をサンプルとして用いて、各カラムタイプの精製コレクションボリューム(PCV)を抽出しました。
その結果、qEV20は、20 nmのサイズ範囲(CPC24;p<0.05)の粒子を多く抽出しており、平均粒子径50 nm (CPC50; p<0.05) や 70 nm (CPC70; p<0.05)においても同様でした。一方で100 nm (CP100)では有意差がないことから、qEV20は粒子径100 nm未満の回収率が向上したことがわかります。
このように、qEV20は、EVをはじめ エクソメアやAAVのような、20~35 nmサイズの粒子抽出に特に適しています。
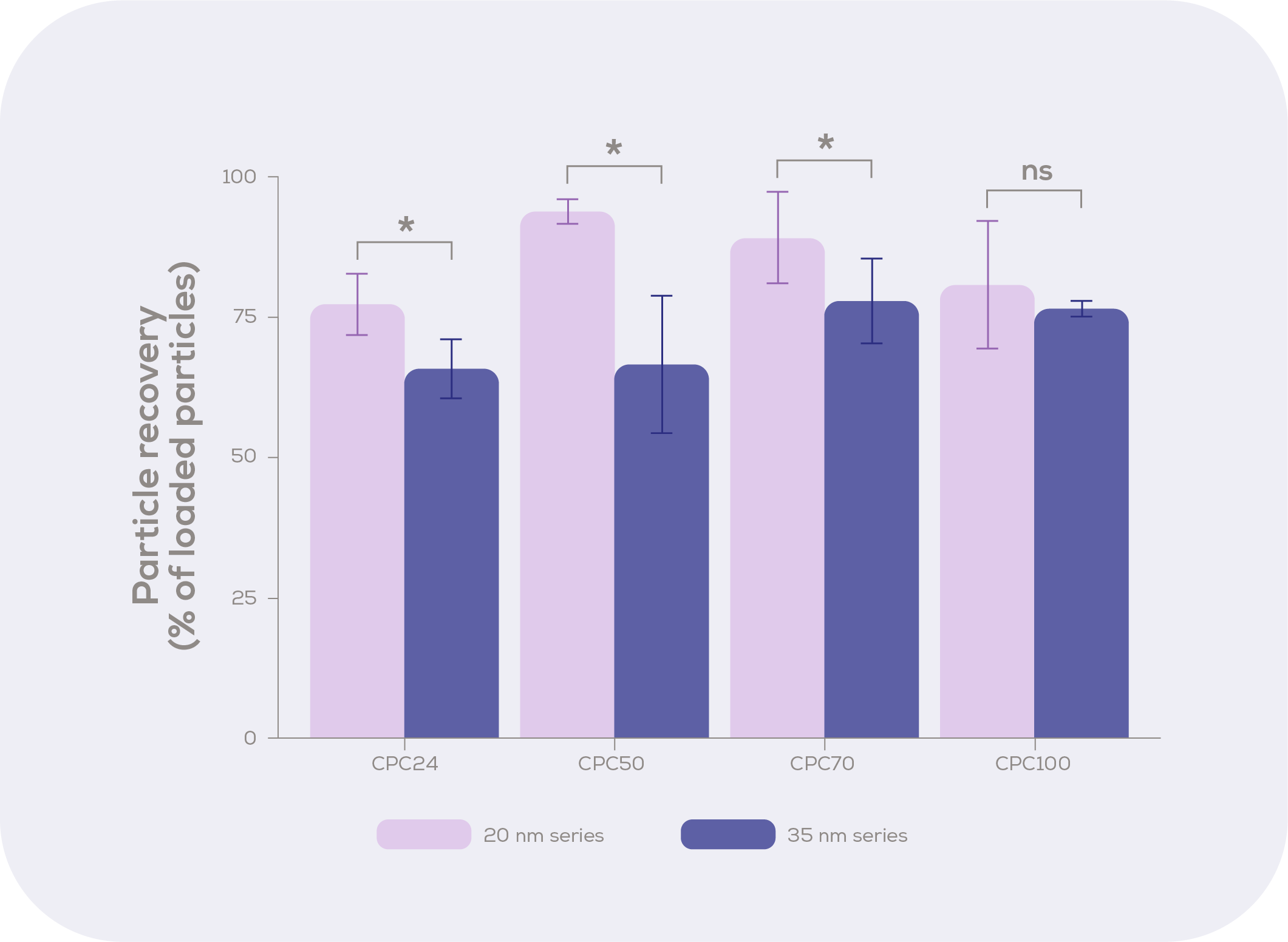
サイズの異なる4種類のカルボキシル化ポリスチレン粒子(CPC)をqEV original/20またはqEV original/35に通し、カラムに指定されたPCVで回収した。回収率は光学密度を用いて測定した。
データは平均±標準誤差を示し、分析はMann-Whitney検定による。* p < 0.05
qEV20は、他のqEVシリーズより多くの粒子を抽出
図2 に示すように、qEV20は、デフォルトのPCVで比較した場合、qEV35(p<0.05)および qEV70 (p<0.01)と比較して2倍以上の粒子を抽出します。つまり、qEV20は、微小粒子をより高効率で抽出したい場合だけでなく、EV収量を優先する場合にも最適な選択肢となり得ます。
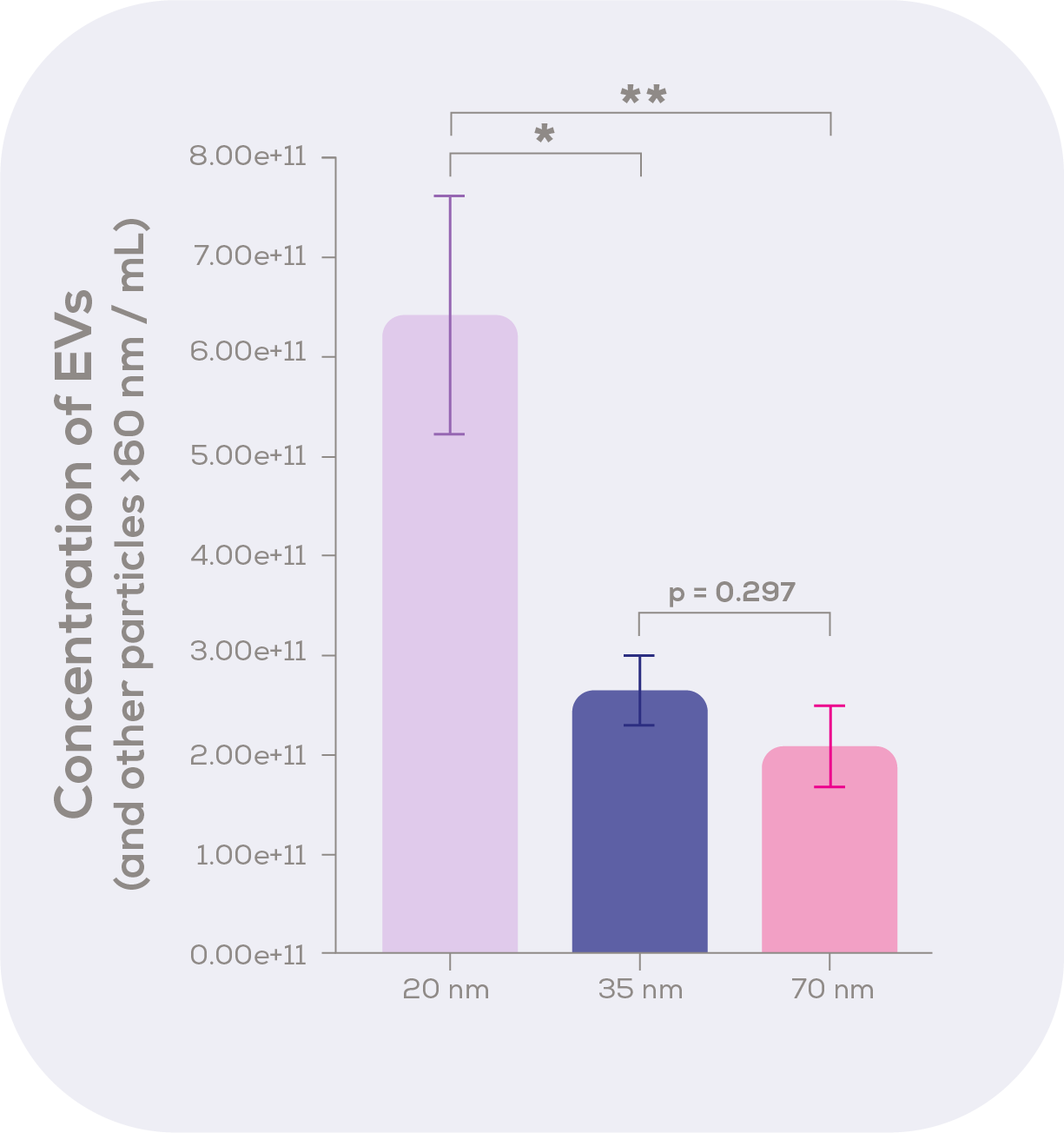
粒子はExoidを用いて測定。データは平均値 ± 標準誤差。
分析はKruskal-Wallis検定とDunnのポストホックテストによる。
* p < 0.05, ** p<0.01
「波形」が表すもの
図 3 では、qEV original / 20 の分析結果を qEV original / 35、qEV original / 70 と並べてプロットしています。この図においてqEV original / 20のタンパク質回収量には特徴的な「波形」があることがわかります。この「波形」は、qEV original / 20を開発した目的の一つであるエクソメアやスーパーメアなどに由来している可能性があり、現在はこの回収物の調査を行っています。
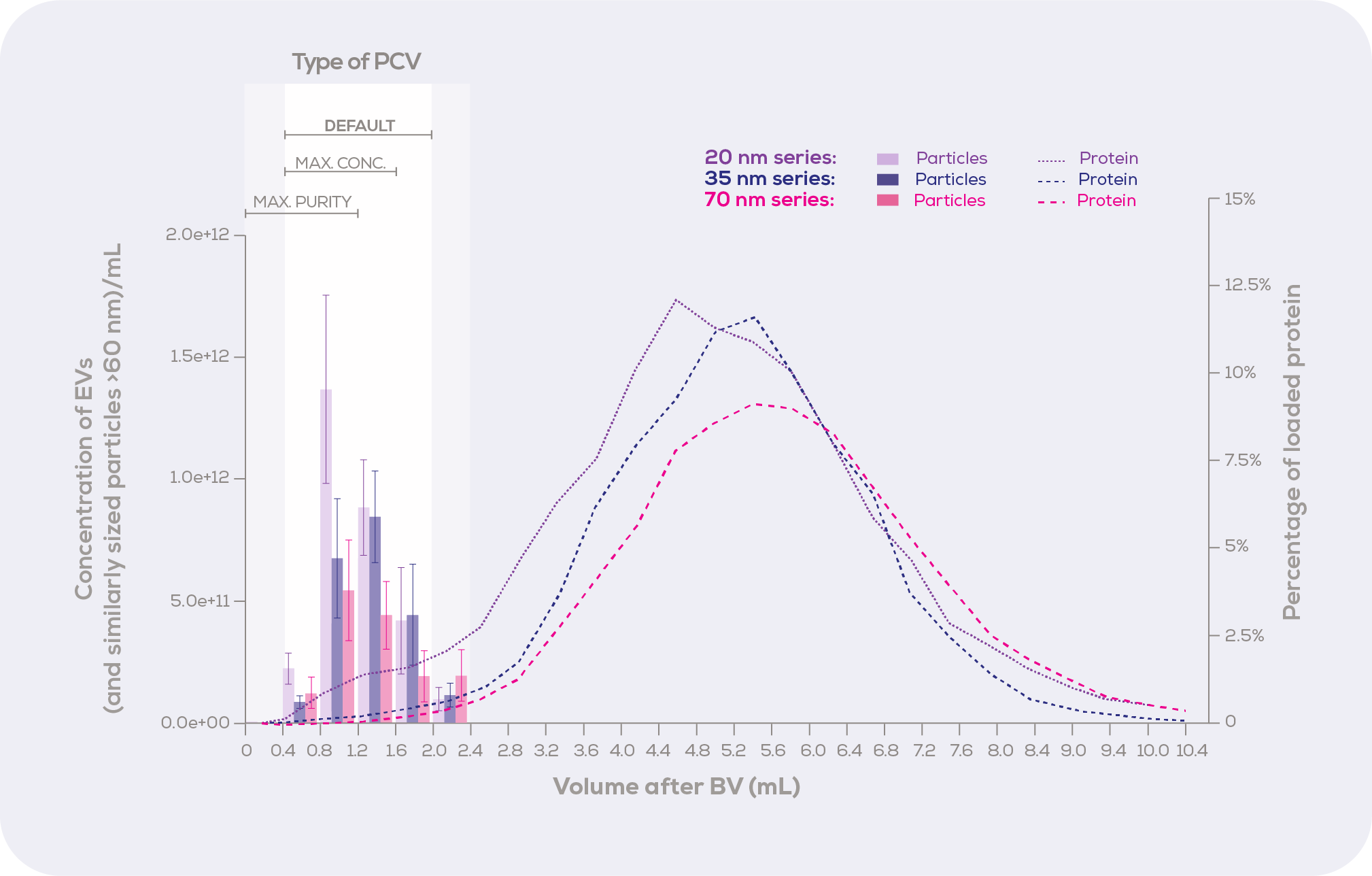
qEV original カラム溶出プロファイル
粒子濃度は Exoid を用いて測定し、タンパク質濃度はビシンコニン酸(BCA)アッセイを用いて測定した。粒子濃度は平均値±標準誤差で表し、タンパク質の回収率は平均値で表した。
タンパク質の「波形」の正体が何であれ、図4 のデータでは、qEV35(p<0.001)および qEV70 (p<0.0001)と比較して、デフォルトPCVでタンパク質収量が増加していることがわかります。
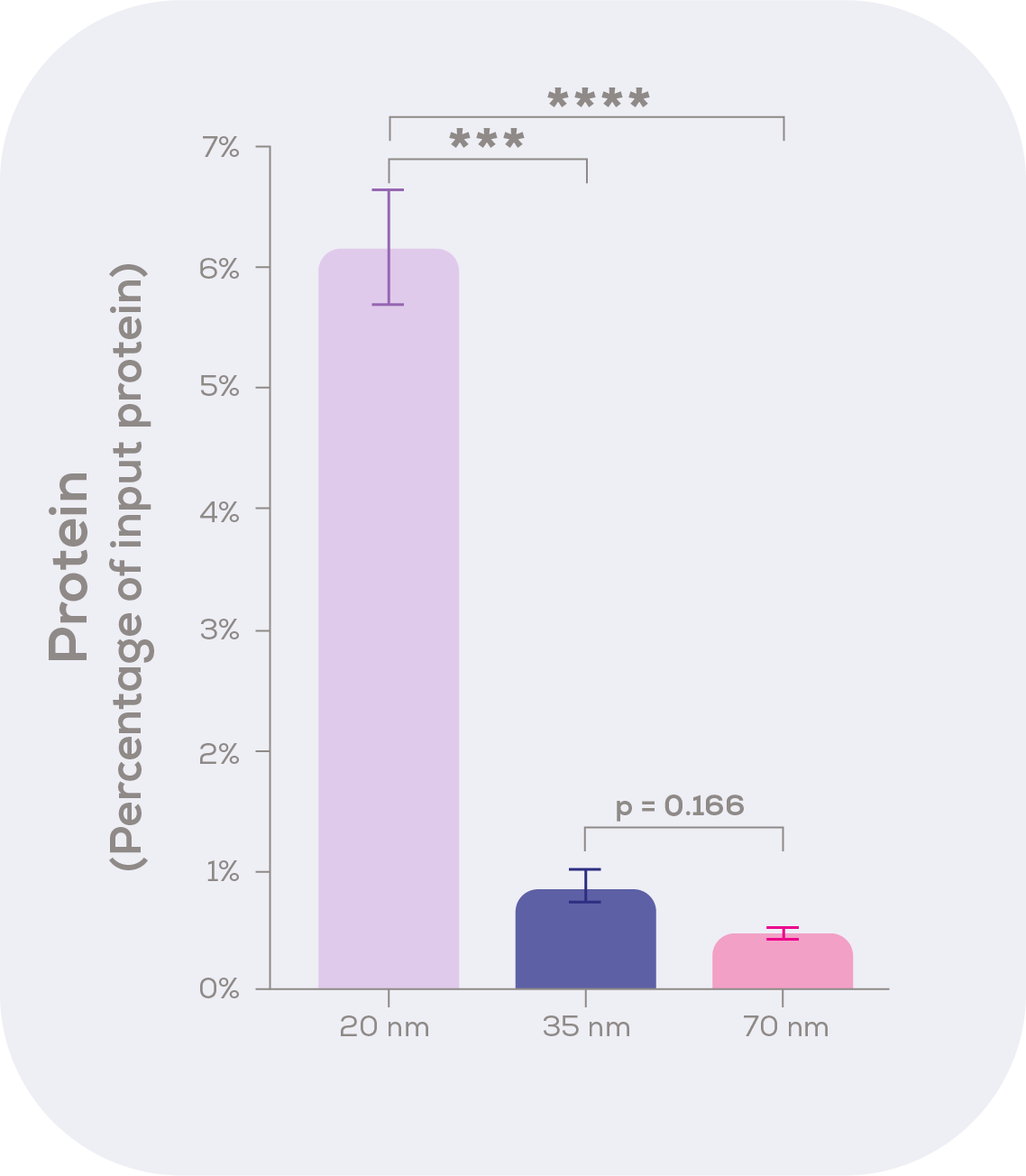
タンパク質濃度はBCAを用いて測定した。データは平均値±標準誤差。
分析はKruskal-Wallis検定とDunnのポストホックテストによる。
*** p < 0.001, **** p<0.0001
qEV20は他の分析法より純度の高い抽出が可能
qEV20による粒子収率の増加は、qEV35(p<0.01)およびqEV70(p<0.01)シリーズのカラムと比較した際の純度の低下をもたらします(図5)。しかし、この純度の低下を加味しても、qEV20は超遠心法、密度勾配超遠心法、沈殿法(血漿/血清の文献比較試験による純度は平均 1e+08 の範囲)などに比べて純度の高い抽出が可能です。
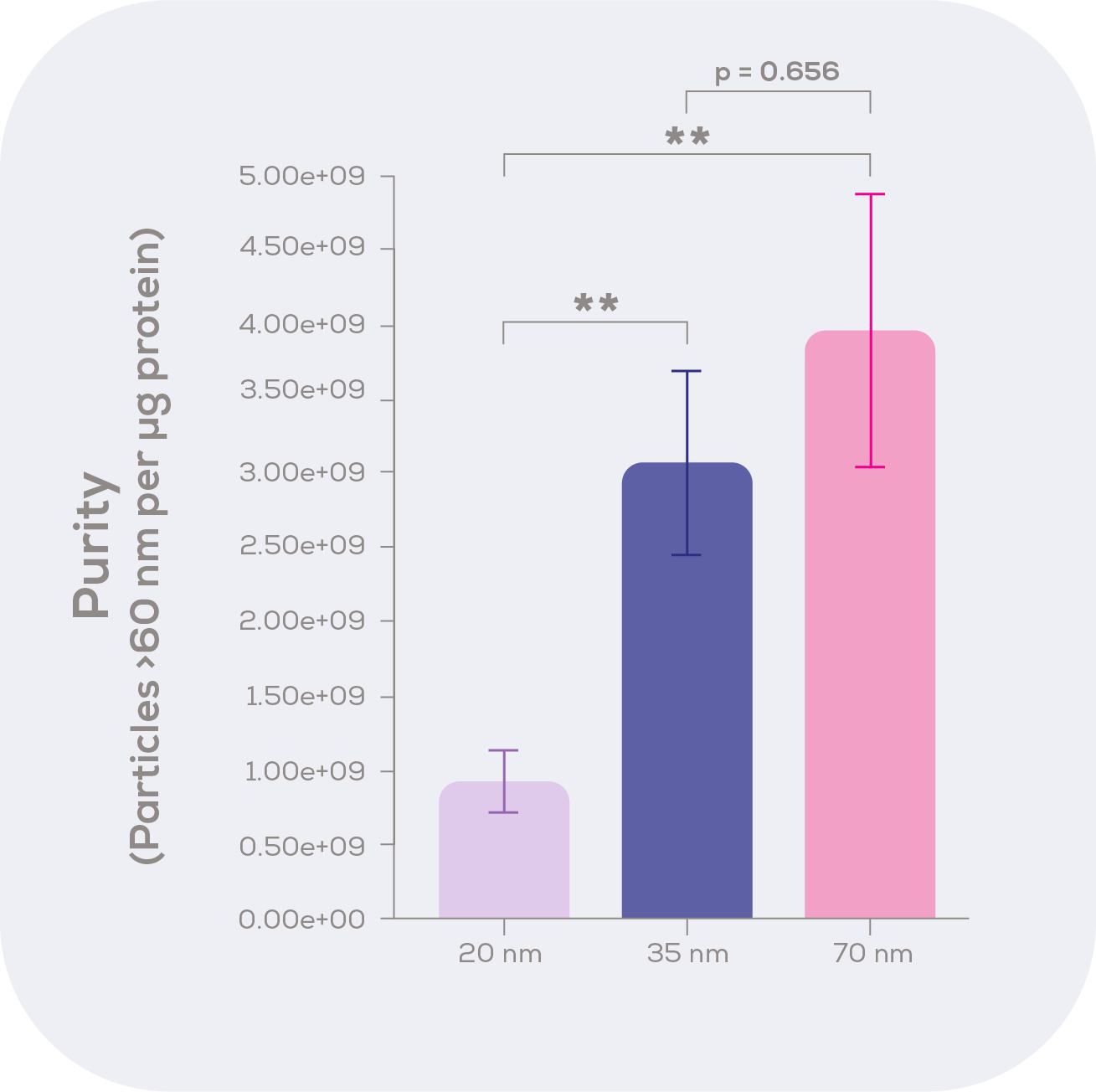
粒子数の測定にはExoidを用い、タンパク質濃度の測定にはBCAアッセイを用いた。
データは平均値±標準誤差、n=13-16。
分析はKruskal-Wallis検定とDunnのポストホックテストによる。** p < 0.01
ナノスケールの発見に必要不可欠なqEV20
qEV20は、small EV、エクソメア、アデノ随伴ウイルスなどの微粒子分離の分野において大きな進歩を遂げています。この技術革新は、ナノ粒子研究での限界を突破するだけでなく、qEVで認知されている高純度基準を維持するためのものです。
qEV20により、これまでアクセスできなかったナノスケールの世界を探索できるようになり、診断や治療における新たな発見の可能性が高まります。
※qEV20 は現在qEV original, qEV10のみご注文いただけます。
他のサイズも順次リリース予定です。詳しくはお問合せ下さい。


